المركَّبات الأيونية تتكوّن من اتّحاد شقّ موجَب (كاتيون) وشقّ سالب (أنيون)، ويتمّ التعبير عن تركيبها باستخدام الصيغة الكيميائية التي توضّح نوع الأيونات وعددها النسبي في المركَّب
لماذا تُكتب الصيغة الكيميائية لكلوريد المغنيسيوم على شكل MgCl2 ؟
عند اتّحاد العناصر لتكوين المركَّبات، تُستخدم طريقة علمية للتعبير
عن نوع وعدد الذرّات في كلّ مركَّب، وتُعرف هذه الطريقة بالصيغة الكيميائية.
كيف يمكن كتابة الصيغة الكيميائية لأي مركَّب أيوني؟
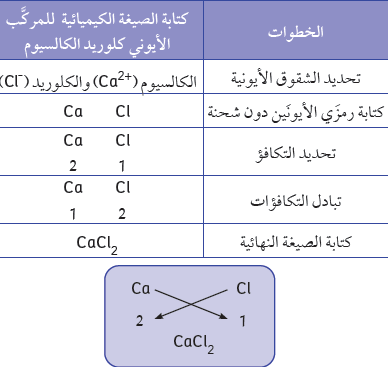
1- كتابة رمز الأيون (الشقّ الأيوني)، حيث يُكتب الأيون موجَب الشحنة جهة اليسار وسالب الشحنة جهة اليمين.
2- يكتب أسفل الرمز التكافؤ.
3- يتمّ تبادل التكافؤ (عملية المقص)، مع الاختصار في حال وجود عامل مشترك.
4- تكتب الصيغة الكيميائية للمركَّب، وإذا كان العدد 1 لا يكتب.
5- تتمّ التسمية اللفظية باللغة العربية، تبدأ بالأيون السالب، ثمّ الأيون الموجَب
خطوات كتابة الصيغة الكيميائية للمركَّب الأيوني باستخدام طريقة تبادل التكافؤات:
أوّلًا : مركَّب كلوريد الكالسيوم:
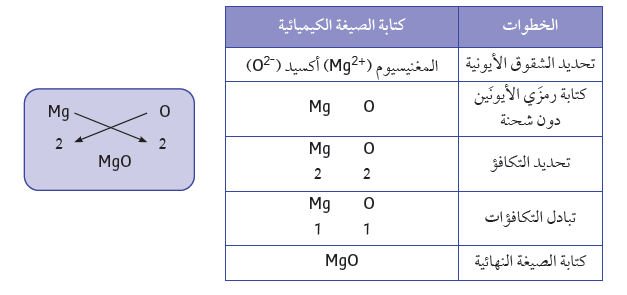
ثانيًا: أكسيد المغنيسيوم
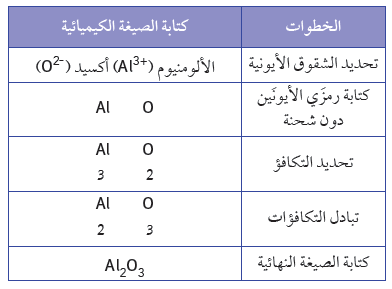
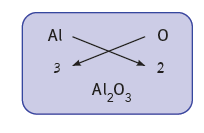
ثالثًا: أكسيد الألومنيوم
إثراء :
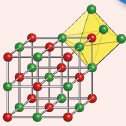
في المركَّبات الأيونية مثل كلوريد لا تتجمَّع ،(NaCl) الصوديوم الذرّات على شكل جُزَيئات منفصلة، بل تنتظم في شبكة بلّورية ثلاثية الأبعاد، تتكرّر فيها الأيونات بشكل منتظم ومتوازن.
في هذه الشبكة، يُحيط بكلّ أيون صوديوم موجب ستة أيونات كلور سالبة و في المقابل يحيط
بكلّ أيون كلور ستّة أيونات صوديوم. يُعرف هذا الترتيب باسم ( التنسيق السداسي ) وهو يعكس
الطريقة التي ترتبط الأيونات في البلّورة لضمان أقصى درجات التجاذب الكهربائي والاستقرار
البنائي.
هذا التكرار المنتظم في البناء يمنح المركَّب صفاته الفيزيائيّة المميَّزة، مثل الصلابة ودرجة الانصهار المرتفعة
مهارة العلوم :
اُذكر: الصيغة الكيميائية للمركَّب الأيوني كلوريد الصوديوم
نشاط :
عند اكتشاف مركَّب أيوني جديد، ما الجهاز أو التقنية المخبرية التي يمكن استخدامها للتحقّق من صحّة
صيغته الكيميائية؟ اِبحث في المصادر الإلكترونية عن اسم الجهاز.
أتحقّق ممّا تعلّمت
السؤال الأوّل: اِختر الإجابة الصحيحة علميًّا لكلّ من العبارات التالية بوضع كلمة صح في المكان المجاور لها:
1- الصيغة الكيميائية الصحيحة لمركَّب يتكوّن من أيون Mg+2 و أيون N-3
(………..) MgN
(………..) MgN2
(………..) Mg3N2
(………..) Mg2N3
2- الغرض من تبادل أعداد التكافؤ (عملية المقصّ) عند كتابة الصيغة الكيميائية:
(………..) لمعرفة أيون الفلزّ وأيون اللافلزّ.
(………..) لتحديد نوع الشقّ الأيوني.
(………..) لمعرفة اسم المركَّب الأيوني.
(………..) لتحديد عدد الذرّات في كتابة الصيغة الكيميائية.
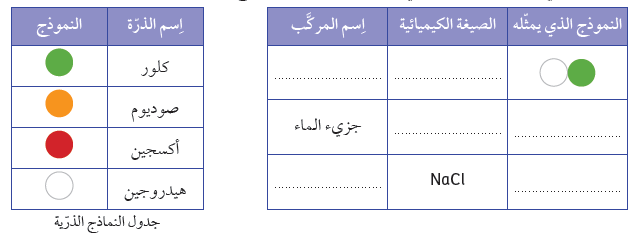
السؤال الثاني: أكمِل الجدول التالي بالاستعانة بجدول النماذج الذرّية: